
В большинстве случаев рак желудка носит спорадический характер, то есть заболевание развивается как будто случайно, без явных причин. Определенные факторы риска, связанные с образом жизни и особенностями питания, удается выявить только во время тщательного сбора анамнеза.
Намного реже – примерно в 10% случаев – злокачественные опухоли желудка развиваются на фоне отягощенного семейного анамнеза, то есть ранее это заболевание было диагностировано у родственников пациента. И только в 1–5% случаев рак желудка явно имеет наследственную причину. Чаще всего высокая предрасположенность к развитию злокачественной опухоли обусловлена синдромом наследственного диффузного рака желудка. Реже встречаются другие генетические синдромы. Идентифицировать их зачастую непросто. Чтобы установить точный диагноз, помимо врача-онколога, может потребоваться участие хирурга, клинического генетика, патоморфолога.
Наследственные нарушения в генах способны влиять на возраст возникновения злокачественных опухолей (обычно они диагностируются у более молодых пациентов), характер течения заболевания, прогноз. В клиниках федеральной сети «Евроонко» доступны все виды генетического тестирования.
Интеллектуальная собственность https://www.euroonco.ru
Причины возникновения
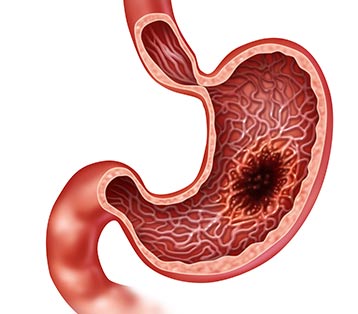
Основная причина развития наследственных злокачественных опухолей в желудке – наследственный диффузный рак желудка (сокращенно HDGC – от англ. hereditary diffuse gastric cancer). Чаще всего этот синдром развивается из-за мутации в гене CDH1. Данный ген кодирует белок под названием E-кадгерин, участвующий в важных процессах:
- регуляция механического взаимодействия между отдельными клетками – клеточной адгезии (иными словами, обеспечивает способность клеток «прилипать» друг к другу);
- передача химических сигналов внутри клеток;
- контроль созревания и передвижения клеток.
E-кадгерин относится к супрессорам опухолевого роста: за счет своих свойств он подавляет развитие и рост злокачественных опухолей. Если его функция из-за мутации нарушается, то клетки не погибают естественным образом, когда приходит время это делать. Они становятся бессмертными и продолжают бесконтрольно размножаться. Иными словами, приобретают свойства злокачественных клеток.
HDGC встречается у 1% людей и повышает риск развития рака желудка в течение жизни до 80%. Мутация наследуется по аутосомно-доминантному типу, то есть для того, чтобы получить HDGC, достаточно унаследовать одну дефектную копию гена от одного из родителей, при этом вторя копия может быть нормальной. Шанс передать мутацию ребенку, если она есть у родителя, составляет 50%. Также HDGC повышает риск развития некоторых других онкологических заболеваний, например, инвазивного лобулярного (долькового) рака молочной железы.
 Определенная роль принадлежит белку p120-катенину, кодируемому геном под названием CTNND1. Этот белок помогает удерживать E-кадгерин на клеточной мембране в нужном месте, не позволяя ему проникать внутрь клетки посредством эндоцитоза и преждевременно разрушаться.
Определенная роль принадлежит белку p120-катенину, кодируемому геном под названием CTNND1. Этот белок помогает удерживать E-кадгерин на клеточной мембране в нужном месте, не позволяя ему проникать внутрь клетки посредством эндоцитоза и преждевременно разрушаться.
Существуют и другие менее распространенные наследственные синдромы, ответственные за развитие злокачественных опухолей желудка:
- Синдром Линча. Другое название – наследственный неполипозный колоректальный рак, сокращенно HNPCC (hereditary non-polyposis colorectal cancer). Представляет собой наследственное заболевание, повышающее риск развития рака желудка, толстой и прямой кишки, некоторых других онкологических заболеваний. Развивается при нарушениях в одном из так называемых генов репарации несоответствия (MMR): обычно MLH1 или MSH2. Белки, кодируемые этими генами, помогают восстанавливать поврежденную ДНК, а при нарушении их функций в клетках накапливается еще больше мутаций. Риск развития злокачественной опухоли в желудке в течение жизни составляет 2–30%.
- Семейный аденоматозный полипоз. У людей с этим генетическим нарушением с раннего возраста возникает множество полипов в толстой кишке, а также иногда в желудке и тонкой кишке. При этом сильно возрастает риск развития колоректального рака, в меньшей степени – вероятность развития злокачественных опухолей желудка. Нарушение вызвано мутацией в гене APC. Риск возникновения злокачественной опухоли составляет 2–4%.
- Аденома желудка и проксимальный полипоз желудка (GAPPS) – редкий синдром, возникающий из-за мутаций в определенных участках гена APC. У таких людей в желудке много полипов и повышен риск развития рака желудка.
- Синдром Ли-Фраумени развивается при мутации в гене TP53, кодирующем белок p53 – «страж генома». Когда ДНК сильно повреждена и не может быть восстановлена, этот белок останавливает клеточные деления и запускает апоптоз – запрограммированную клеточную смерть. Если белок не работает, то клетки с поврежденной ДНК выживают и могут стать раковыми. При синдроме Ли-Фраумени повышается риск развития целого ряда онкологических заболеваний, в том числе рака желудка (около 5% в течение жизни), в относительно молодом возрасте.
- Синдром Пейтца-Егерса. Проявляется в виде полипов в желудке, кишечнике, носу, дыхательных путях, мочевом пузыре. Полипы в пищеварительном тракте называются гамартомами. Они способны привести к кровотечению, кишечной непроходимости. Нередко синдром Пейтца-Егерса приводит к появлению темных пятен на губах, внутренней поверхности щек и в других местах. У таких людей повышен риск развития злокачественных опухолей желудка, рака толстой кишки, поджелудочной железы, груди. Причиной становится мутация в гене STK11. Риск развития рака желудка при этом составляет около 30%.

Лечение наследственного рака желудка
Лечение злокачественных опухолей желудка, связанных с наследственными генетическими синдромами, зависит от стадии, характера течения заболевания, возраста, общего состояния здоровья пациента и других факторов.
Хирургия
При HDGC обычно желудок удаляют полностью – выполняют тотальную гастрэктомию. Это помогает максимально снизить риск рецидива. Также обычно удаляют много близлежащих лимфатических узлов – нередко проводят лимфодиссекцию D2. В конце операции накладывают анастомоз между оставшимися концами пищевода и двенадцатиперстной кишки.
Противоопухолевая терапия
Химиопрепараты применяют в разных режимах:
- Неоадъювантная терапия проводится перед операцией, чтобы уменьшить размеры злокачественного новообразования, упростить его удаление, сократить объем хирургического вмешательства.
- Адъювантная химиотерапия проводится после удаления опухоли, чтобы уничтожить оставшиеся в организме раковые клетки и снизить риск рецидива.
- В качестве основного метода лечения химиопрепараты применяют при заболевании на поздней стадии. Они помогают затормозить прогрессирование злокачественной опухоли, улучшить состояние больного, продлить жизнь.
В определенных случаях применяют современные таргетные препараты, иммунопрепараты из группы ингибиторов контрольных точек.
Лучевая терапия
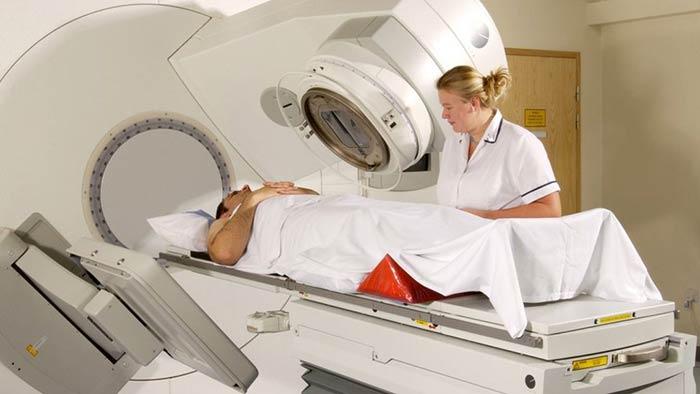
Лучевую терапию, как и химиотерапию, проводят в качестве адъювантного, неоадъювантного или основного лечения при поздних стадиях. Благодаря современным технологиям, таким как трехмерная конформная лучевая терапия (3D-CRT) и лучевая терапия с модулированной интенсивностью (IMRT), можно максимально прицельно облучать злокачественное новообразование, воздействовать на него максимально высокими дозами и при этом практически не затрагивать окружающие здоровые ткани.
Прогноз и профилактика
Можно заранее прогнозировать вероятность того, что ребенок получит дефектные гены, если провести генетические анализы у будущих родителей на этапе планирования беременности. Если же у человека уже обнаружен один из перечисленных выше синдромов, поделать с этим ничего не получится. Но можно принять некоторые меры, чтобы защитить себя.
В качестве скринингового исследования применяется гастроскопия. Во время нее врач вводит в желудок фиброскоп с видеокамерой, осматривает слизистую оболочку, может провести биопсию подозрительных участков. Как показывает статистика, во время эндоскопических исследований диффузный рак на ранних стадиях часто пропускают, поэтому скрининг должен проводить врач, который специализируется на работе с такими пациентами и обладает соответствующим опытом.
Единственный эффективный метод профилактики развития злокачественной опухоли при HDGC – профилактическая тотальная гастрэктомия. Однако эта операция сама по себе весьма травматична, после нее необратимо и сильно меняется пищеварение, придется соблюдать диету.
Помимо врожденных нарушений в генах, существует множество других факторов риска развития онкозаболеваний. Многие из них связаны с образом жизни, внешними воздействиями, и от них себя вполне можно оградить, тем самым дополнительно несколько снизив риски.
В клиниках федеральной сети «Евроонко» можно получить консультацию одного из ведущих врачей-онкологов, пройти комплексное скрининговое обследование, гастроскопию с применением эндоскопического оборудования высокого разрешения, без боли и дискомфорта, в состоянии «медикаментозного сна». Мы применяем современные методы лечения злокачественных опухолей, строго придерживаемся принципов доказательной медицины и следуем последним версиям международных протоколов, рекомендациям авторитетных международных онкологических ассоциаций. Мы знаем, как помочь.



























