- Почему возникает канцероматоз брюшины?
- В чем преимущества гипертермической интраперитонеальной химиотерапии?
- Как проводят процедуру?
- Ревизия
- Циторедуктивная операция
- Гипертермическая интраперитонеальная перфузия
- Какие химиопрепараты применяют для HIPEC?
- Реконструкция
- Риски и возможные осложнения
- При каких других типах рака применяют методику?
- Насколько хорошо изучена HIPEC? Доказана ли эффективность?
- Каков прогноз?
Гипертермическая интраперитонеальная химиотерапия (HIPEC — от англ. Hyperthermic IntraPeritoneal Chemotherapy) — инновационный метод лечения в онкологии, который предполагает введение в брюшную полость химиопрепарата, нагретого до 42–43 °C. Ее применяют при канцероматозе (поражении раковыми клетками) брюшины.
Благодаря появлению HIPEC, стало возможным лечение злокачественных опухолей, которые ранее считались неоперабельными.
Интеллектуальная собственность https://www.euroonco.ru
Почему возникает канцероматоз брюшины?
Брюшина представляет собой тонкую пленку из соединительной ткани. Она выстилает изнутри брюшную полость, покрывает внутренние органы. Некоторые органы покрыты брюшиной со всех сторон (расположены интраперитонеально), другие — частично (мезоперитонеально) или только с одной стороны (экстраперитонеально). [1,2]
На поздних стадиях некоторых онкологических заболеваний раковые клетки могут распространяться в брюшину и проникать в брюшную полость, давать начало вторичным очагам. При этом резко ухудшается прогноз, снижается эффективность противоопухолевого лечения, так как многие препараты при внутривенном введении плохо проникают через брюшину.
Наиболее распространенные причины поражения брюшины раковыми клетками:
- Рак яичника — в 60% случаев. [3,4]
- Колоректальный рак (аденокарцинома толстой и прямой кишки) приводит к канцероматозу брюшины в 15% случаев.
- Рак желудка — в 50% случаев. [5]
- Рак аппендикса (аппендикулярная карцинома).
- Рак молочной железы.
- Рак поджелудочной железы.
- Псевдомиксома брюшины — редкая злокачественная опухоль, которая, как правило, начинается в аппендиксе. Реже первичный очаг может находиться в кишечнике, яичнике, мочевом пузыре. Опухолевые клетки производят желеобразную жидкость — муцин — которая со временем накапливается в брюшной полости. При отсутствии лечения больной погибает от кишечной непроходимости, истощения.
- Перитонеальная мезотелиома — редкая злокачественная опухоль, которая изначально развивается в брюшине. [6]
Асцит брюшины, который часто сопровождает канцероматоз, проявляется увеличением объёма и болями в животе, потерей аппетита, тошнотой и рвотой. Из-за нарастания асцита (скопления жидкости в брюшной полости) нарушается работа кишечника и других органов, возникает одышка. Зачастую поражение брюшины не вызывает каких-либо симптомов и обнаруживается только во время хирургического вмешательства.
В диагностике канцероматоза брюшины помогают такие исследования, как компьютерная томография, ПЭТ-КТ, биопсия, диагностическая лапароскопия, анализ крови на онкомаркеры.
В чем преимущества гипертермической интраперитонеальной химиотерапии?
Ранее пациентов, у которых был диагностирован канцероматоз брюшины, часто признавали безнадежными. Классические методы лечения рака (хирургия, системная химиотерапия, лучевая терапия) не могли продлить жизнь таких больных. Выживаемость измерялась неделями и месяцами. За последние два десятилетия ситуация изменилась.
HIPEC обладает преимуществами, которые помогли существенно повысить эффективность борьбы с поражением брюшины раковыми клетками:
- Гипертермическая интраперитонеальная химиотерапия — это локальное воздействие. Препарат вводят непосредственно в место, где находятся очаги, он не поступает в общий кровоток. Это позволяет увеличить дозу до десятикратной, не опасаясь серьезных побочных эффектов.
- Опухолевые клетки получают сразу «двойной удар». Помимо химиопрепарата, на них действует повышенная температура. Нагревание повреждает мембрану и внутренние структуры опухолевых клеток, вызывает апоптоз (запрограммированную клеточную смерть), изменяет пространственную структуру ДНК и нарушает ее репарацию, усиливает эффект химиопрепаратов.
- Зачастую клетки внутри опухоли находятся в состоянии гипоксии — кислородного голодания. При этом снижается эффективность лучевой терапии. Но такие опухолевые клетки чувствительны к высокой температуре.
- В очагах небольшого размера (до 3 мм) практически не происходит ангиогенез (процесс образования новых кровеносных сосудов в ткани). Из-за этого они недоступны для системной химиотерапии. HIPEC помогает решить эту проблему. Благодаря нагреванию, препарат проникает в опухолевую ткань на глубину до 3 мм. Это помогает эффективно уничтожать раковые клетки. [7]
Как проводят процедуру?
Лечение состоит из четырех этапов:
- Ревизия (осмотр) брюшной полости.
- Циторедуктивная операция.
- Собственно HIPEC.
- Реконструкция.
Вмешательство сложное и длительное, оно может продолжаться до 16 часов (в среднем — 3–9 часов).
Ревизия
Во время ревизии хирурги тщательно осматривают брюшную полость. Оценивают перитонеальный индекс рака (peritoneal cancer index, сокращенно — PCI). Брюшную полость условно делят на 13 областей. В каждой из них оценивают размеры самого большого узла. В зависимости от этого каждая область получает определенное количество баллов:
- узел не визуализируется — 0 баллов;
- менее 0,5 см — 1 балл;
- 0,5–5 см — 2 балла;
- узел более 5 см или несколько сливающихся более мелких узлов — 3 балла.
Врачи должны убедиться, что смогут удалить все видимые узлы. Прогноз оценивают в зависимости от общей суммы баллов и типа опухоли. Если сумма превышает критическое значение, лечение признают нецелесообразным. Операцию завершают, HIPEC отменяют. Перитонеальный индекс рака можно также оценить в ходе диагностической лапароскопии на этапе обследования. [8,9]
Циторедуктивная операция
Во время циторедуктивной операции нужно удалить все видимые очаги размерами более 1–2 мм. От того, насколько качественно это сделано, зависит эффективность всего лечения и прогноз для пациента. Удаляют орган, в котором находится опухоль, или его пораженную часть, париетальную (выстилающую стенки брюшной полости) и часть висцеральной (покрывающей внутренние органы) брюшины, соседние пораженные органы. [8,9]
Гипертермическая интраперитонеальная перфузия
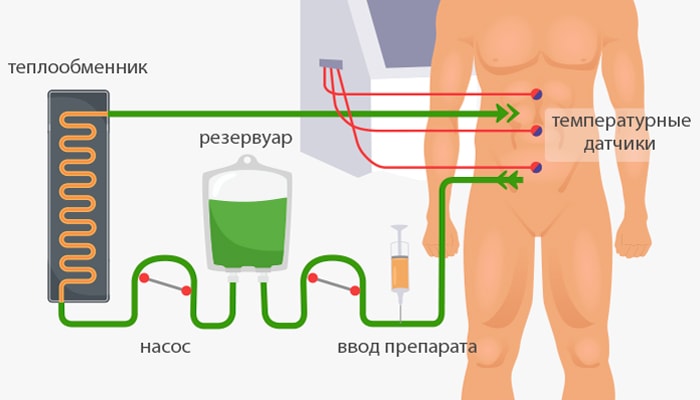
После операции все видимые опухоли удалены, но в брюшной полости все еще остались раковые клетки. Если эти клетки не будут уничтожены, они дадут начало новым очагам, произойдет рецидив, и весь эффект от лечения будет сведен на нет. Эту задачу и помогает решить HIPEC.
Через катетеры, подсоединенные к специальному аппарату, брюшную полость пациента промывают раствором химиопрепарата, подогретым до 42–43 °C. Процедура продолжается 30–90 минут, после чего раствор полностью удаляют из брюшной полости. Постоянно контролируют скорость потока, давление, объем раствора. В теле пациента во время процедуры установлены температурные датчики.
Какие химиопрепараты применяют для HIPEC?
Чаще всего в брюшную полость вводят митомицин C, оксалиплатин и цисплатин. Нагревание повышает эффективность таких химиопрепаратов, как карбоплатин, митоксантрон, доксорубицин, эпирубицин, ифосфамид. [8,9]
Реконструкция
После того как все очаги удалены, хирург восстанавливает целостность кишечника, если это невозможно — накладывает еюно-, цеко- или колостому: подшивает к коже подвздошную, слепую или ободочную кишку и формирует отверстие для отхождения стула.
Пациент перенес серьезное хирургическое вмешательство, поэтому на некоторое время его помещают в палату интенсивной терапии. [8,9]

Риски и возможные осложнения
Циторедуктивная операция в сочетании с HIPEC — сложное вмешательство. Оно несет определенные риски. Смертность от осложнений после лечения составляет 3%. Это ниже, чем при многих других сложных операциях.
После хирургического вмешательства возможны некоторые осложнения:
- Инфекции легких и мочевого пузыря.
- Осложнения в месте операционной раны.
- Сложности с приемом пищи и жидкости в течение нескольких дней.
- Редко встречаются инфекции брюшной полости и выпадение волос.
Срок госпитализации в среднем составляет 2–4 недели. Спустя несколько недель проводится контрольное обследование. Затем его повторяют через каждые 3 месяца, постепенно частоту уменьшают до 1 раза в год.
При каких других типах рака применяют методику?
Подогретые растворы химиопрепаратов можно вводить не только в брюшную полость. Существует такая процедура, как изолированная гипертермическая перфузия (LIMB). Химиопрепарат вводят в артерию ноги или руки. LIMB помогает спасти конечность от ампутации при меланомах, саркомах мягких тканей.
Насколько хорошо изучена HIPEC? Доказана ли эффективность?
HIPEC помогает существенно увеличить продолжительность жизни и улучшить состояние пациентов — это доказано в ходе научных исследований.
Семьдесят два ведущих хирурга-онколога из 55 онкологических центров в 14 странах мира, включая США, пришли к выводу о том, что HIPEC может существенно повысить ожидаемую продолжительность жизни у пациентов, страдающих раком толстой и прямой кишки.

Каков прогноз?
Если лечение при канцероматозе брюшины не проводится, средняя выживаемость пациентов составляет всего 2–6 месяцев. HIPEC в сочетании с циторедуктивной операцией помогает существенно улучшить прогноз. Средняя выживаемость после лечения измеряется годами. Фактически HIPEC способна полностью уничтожить опухоль, но впоследствии может возникнуть рецидив. [10-12]
С целью предотвращения рецидива и метастазирования через 4–6 недель после хирургического лечения и HIPEC может быть назначен курс адъювантной химиотерапии.
Список литературы:
- Соломенный Сергей Владимирович, Ганцев Камиль Шамилевич, Кзыргалин Шамиль Римович, Минигазимов Рамиль Султанович Анатомические предпосылки развития и особенности течения канцероматоза брюшины // Ульяновский медико-биологический журнал. 2016. №3.
- Р. Ш. Ишмуратова, Ш. Р. Кзыргалин, К. Ш. Ганцев, Р. С. Минигазимов, С. В. Соломенный, Л. В. Халикова Анатомические предпосылки развития перитонеального канцероматоза. Анализ литературы и собственные данные // Креативная хирургия и онкология. 2013. №3.
- Deraco М., Gomez E., Baratti D., Kusamura S., Ter-Ovanesov M. Гипертермическая интраперитонеальная химиоперфузия (HIPEC) в лечении интраперитонеально диссеминированного рака яичников // Злокачественные опухоли. 2012. №2.
- Шелехов Алексей Владимирович, Дворниченко Виктория Владимировна, Радостев Сергей Иванович, Мориков Дмитрий Дмитриевич, Расулов Родион Исмагилович, Ушакова Ирина Викторовна, Медведников Андрей Александрович, Захаров Антон Геннадьевич, Демонов Роман Николаевич, Гладкова Ольга Владимировна, Чернорубашкина Наталья Михайловна Опыт применения технологии циторедуктивной хирургии с методом интраоперационной интраперитонеальной гипертермической химиотерапии в лечении больных распространенным раком яичников // Сибирский онкологический журнал. 2018. №3.
- Давыдов Михаил Иванович, Тер-ованесов Михаил Дмитриевич, Буйденок Юрий Владимирович, Полоцкий Борис Евсеевич, Горбунова Вера Андреевна, Абдуллаев Амир Гусейнович Гипертермическая интраоперационная интраперитонеальная химиотерапия при раке желудка: существует ли реальная возможность изменить прогноз? // Вестн. РОНЦ им. Н. Н. Блохина РАМН. 2010. №1.
- Federico Coccolini, Federico Gheza, Marco Lotti, Salvatore Virzì, Domenico Iusco, Claudio Ghermandi, Rita Melotti, Gianluca Baiocchi, Stefano Maria Giulini, Luca Ansaloni, and Fausto Catena. Peritoneal carcinomatosis. World J Gastroenterol. 2013 Nov 7; 19(41): 6979–6994. Published online 2013 Nov 7. doi: 10.3748/wjg.v19.i41.6979.
- Информационный портал mesotheliomahope.com.
- Mohammed Ben Aziz; Raffaela Di Napoli. Hyperthermic Intraperitoneal Chemotherapy. Treasure Island (FL): StatPearls Publishing; 2021 Jan-.
- S. J. Valle, N. A. Alzahrani, W. Liauw, P. H. Sugarbaker, A. Bhatt, and D. L. Morris. Hyperthermic Intraperitoneal Chemotherapy (HIPEC) Methodology, Drugs and Bidirectional Chemotherapy. Indian J Surg Oncol. 2016 Jun; 7(2): 152–159. Published online 2016 Feb 5. doi: 10.1007/s13193-016-0498-0.
- Guyu Zhang, Yimin Zhu, Chongdong Liu, Guangming Chao, Ran Cui, and Zhenyu Zhang. The prognosis impact of hyperthermic intraperitoneal chemotherapy (HIPEC) plus cytoreductive surgery (CRS) in advanced ovarian cancer: the meta-analysis. J Ovarian Res. 2019; 12: 33. Published online 2019 Apr 17. doi: 10.1186/s13048-019-0509-1.
- Stefaan Mulier, Jean-Pierre Claes, Vincent Dierieck, Jean-Olivier Amiel, Jean-Philippe Pahaut, Luc Marcelis, Fabienne Bastin, Denis Vanderbeeken, Claude Finet, Sophie Cran, Thierry Velu. Survival benefit of adding Hyperthermic IntraPEritoneal Chemotherapy (HIPEC) at the different time-points of treatment of ovarian cancer: review of evidence. Curr Pharm Des. 2012;18(25):3793-803. doi: 10.2174/138161212802002616.
- Franco Roviello , Enrico Pinto, Giovanni Corso, Corrado Pedrazzani, Stefano Caruso, Marco Filippeschi, Roberto Petrioli, Stefania Marsili, Maria Antonietta Mazzei, Daniele Marrelli. Safety and potential benefit of hyperthermic intraperitoneal chemotherapy (HIPEC) in peritoneal carcinomatosis from primary or recurrent ovarian cancer. J Surg Oncol. 2010 Nov 1;102(6):663-70. doi: 10.1002/jso.21682.